[경제일보] GC녹십자가 차세대 혈우병 치료제 개발을 전격 중단하고 ‘선택과 집중’ 전략을 택했다.글로벌 제약사 화이자가 동일 기전의 신약으로 국내 시장 선점에 나서면서 막대한 비용이 소요되는 후속 임상 대신 성공 가능성이 높은 다른 희귀질환 치료제에 역량을 집중하려는 실리적 판단으로 풀이된다.
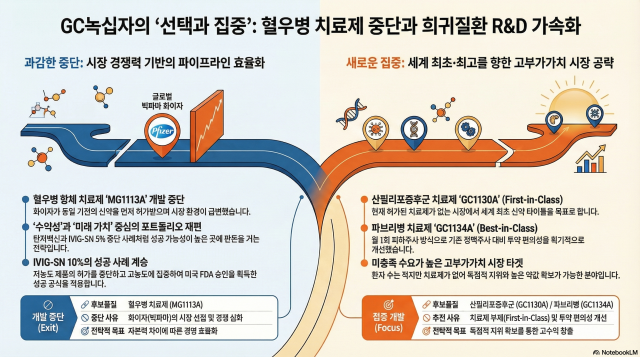
24일 업계에 따르면 GC녹십자는 최근 임상 1b상 단계에 있던 A·B형 혈우병 항체 치료제 후보물질 ‘MG1113A’의 개발 중단을 확정했다. 업계에서는 이를 두고 "안 되는 패는 과감히 버리고 이길 수 있는 판에 판돈을 몰아주는 전형적인 파이프라인 효율화 전략"이라는 평가가 나온다.
혈우병은 혈액 내 응고인자가 부족해 지혈이 되지 않는 유전성 질환이다. 그간 환자들은 부족한 응고인자를 보충하기 위해 주 2~4회 정맥주사를 맞아야 하는 번거로움을 견뎌왔다. GC녹십자가 개발해온 ‘MG1113A’는 혈액 응고를 방해하는 단백질(TFPI)을 억제해 피가 잘 굳게 만드는 원리로 주 1회 피하주사(복부나 허벅지 주사)만으로도 효과를 볼 수 있어 차세대 ‘게임 체인저’로 기대를 모았다.
하지만 시장 환경이 급변했다. 글로벌 빅파마인 한국화이자제약의 혈우병 신약 ‘하임파지’가 지난달 식품의약품안전처로부터 품목 허가를 획득하며 국내 시장에 먼저 깃발을 꽂은 것이다. 하임파지는 GC녹십자의 후보물질과 동일한 ‘TFPI 저해’ 기전을 가진 치료제다.
사실 GC녹십자의 이 같은 ‘과감한 중단’은 이번이 처음이 아니다. 가장 대표적인 사례가 20여 년간 공들여온 탄저백신 ‘GC1109’다. 대테러 대응 등을 위해 국가 과제로 추진됐던 탄저백신은 임상 2상까지 마쳤으나 시장 수요의 불확실성과 임상 설계의 어려움 등으로 결국 사업화 문턱에서 멈춰 섰다. 당시 녹십자는 막대한 연구비를 투입했음에도 불구하고 수익성이 담보되지 않는 사업을 끝까지 끌고 가기보다는 미래 가치가 높은 백신 포트폴리오로 재편하는 길을 택했다.
미국 시장 진출의 상징이었던 면역글로불린 ‘IVIG-SN 5%’의 사례도 빼놓을 수 없다. 당초 녹십자는 농도가 낮은 5% 제품으로 미국 시장의 문을 두드렸으나 현지 시장이 고농도인 10% 제품 위주로 빠르게 재편되자 과감히 5% 제품의 미국 허가 절차를 중단했다. 대신 모든 역량을 10% 제품 개발에 쏟아부었고 그 결과 지난해 말 FDA로부터 품목 허가를 받아내는 쾌거를 거뒀다.
GC녹십자는 ‘산필리포증후군(MPS IIIA)’과 ‘파브리병’ 치료제 개발에 집중한다. 두 질환 모두 환자 수는 적지만 마땅한 치료제가 없어 약값이 매우 비싸고 독점적 지위를 누릴 수 있는 고부가가치 시장이다.
특히 기대를 모으는 것은 산필리포증후군 A형 치료제 ‘GC1130A’다. 이 병은 특정 효소 결핍으로 지적 장애와 신체 퇴행이 일어나는 치명적인 유전병이지만 현재 전 세계적으로 허가된 치료제가 전혀 없다. GC녹십자는 이 분야에서 ‘퍼스트 인 클래스(세계 최초 신약)’ 타이틀을 거머쥐겠다는 복안이다. 현재 한국과 미국에서 동시에 임상 1상을 진행하며 속도를 높이고 있다.
파브리병 치료제 ‘GC1134A’ 역시 유망주다. 기존 치료제들이 정맥주사 방식인 것과 달리 월 1회 피하주사만으로 치료가 가능하도록 편의성을 획기적으로 개선했다. 미국 식품의약국(FDA)과 국내 식약처로부터 이미 희귀의약품(Orphan Drug) 지정을 받아 세제 혜택과 독점 판매권 확보 등 유리한 고지를 점했다.
한 업계 관계자는 “모든 파이프라인을 끝까지 끌고 가기엔 국내 제약사와 글로벌 빅파마 간의 자본력 차이가 너무 크다”며 “글로벌 시장에서 경쟁력이 떨어지는 후보물질을 조기에 정리하는 경영 효율화의 과정”이라고 말했다.
Copyright © 경제일보, 무단전재·재배포 금지









![[현장] 압구정5구역 수주전 가보니…현대건설 미래주거 vs DL이앤씨 자산가치](https://image.ajunews.com/content/image/2026/05/19/20260519115116615313_388_136.png)
![[현장] 유아이패스, 에이전틱 AI 자동화 플랫폼 한국 리전 출시…금융·공공 AI 자동화 시장 공략](https://image.ajunews.com/content/image/2026/05/19/20260519122920975519_388_136.jpg)